[생물학] 5.3~5.4 - Lipids, Proteins
Lipids(지질)
지질은 hydrophobic(소수성)한 생체 분자들을 총칭한다. 주로 극성이 없는 C-H 결합으로 이루어져 있기 때문에 물과 잘 섞이지 않는다. 생체 내에서 중요한 지질에는 지방, 인지질, 스테로이드가 있다.
Fats(지방)
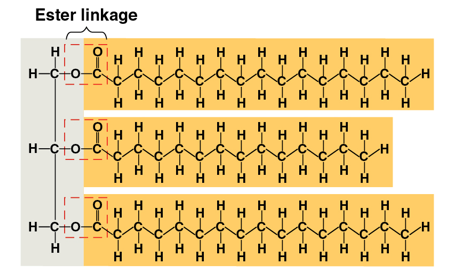
지방은 중합체는 아니지만, 더 작은 분자들의 결합으로 이루어져 있다. glycerol(글리세롤)과 fatty acid(지방산)이 결합하는데, 글리세롤의 hydroxyl group과 지방산의 carboxyl group이 탈수 반응을 거쳐 ester bond(에스터 결합)을 이루게 된다.
위 사진과 같이 글리세롤 1분자와 지방산 3분자가 결합하면 지방이 만들어진다. 혹은 이것을 triglyceride(트라이글리세라이드)라고 부른다. 지방의 주요한 기능은 생명체 안에서 에너지를 저장하는 것이다. (같은 질량의 다당류보다 2배 이상의 에너지를 저장한다)
Saturated vs Unsaturated fat
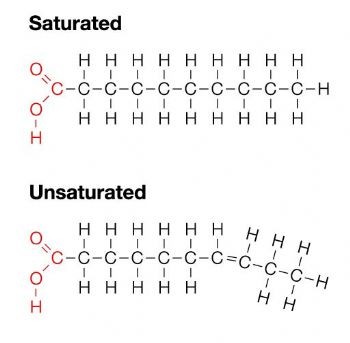
지방산의 탄소 골격에서 탄소 분자들끼리 이중 결합이 없고 수소의 개수가 최대한으로 채워져 있으면, 이것을 saturated fatty acid(포화 지방산)이라고 한다. 반면 탄소의 cis 이중 결합이 있는 지방산은 unsaturated fatty acid(불포화 지방산)이라 한다.
이런 분자 구조의 차이는 지방의 특성에 영향을 미친다. 예를 들어, 포화 지방으로 이루어진 버터와 다르게, 불포화 지방으로 이루어진 올리브유는 구부러진 모양으로 인해 지방 분자들이 일정하게 정렬하기 어려워 상온에서 응고하지 않는다. 한편, 탄소의 trans 이중 결합이 있는 지방산은 trans unsaturated fatty acid라고 한다. 이것이 trans fat(트랜스 지방)에 들어 있는 분자이다. 이것이 혈관에 축적되면 심혈관계 질환을 일으킬 수 있는 것으로 알려져 있다.
saturated fatty acid, unsaturated fatty acid, trans unsaturated fatty acid의 예시로는 각각 stearic acid, oleic acid, elaidic acid가 있다.
Phospholipids(인지질)
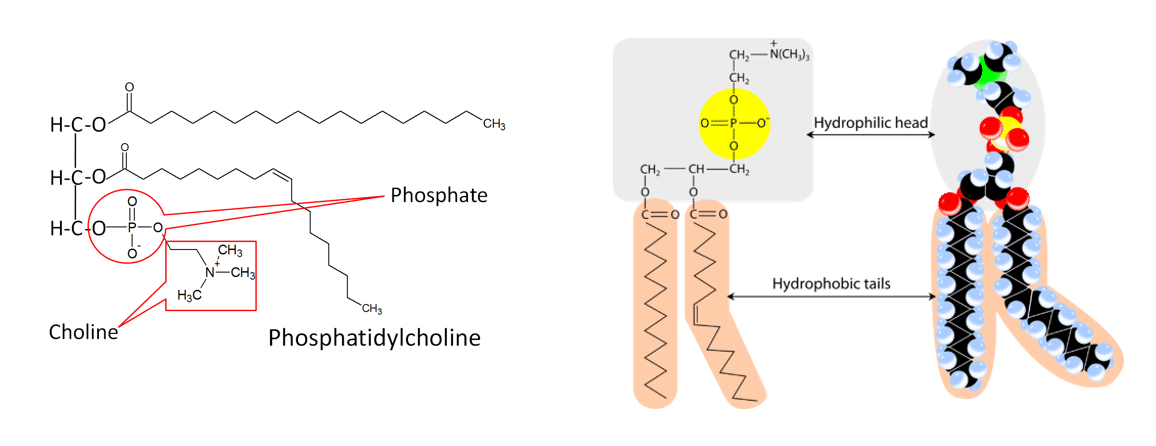
세포막을 구성하는 인지질은 세포에게 있어 필수적인 지질이다. 인지질의 글리세롤은 지방의 글리세롤과 다르게 2분자의 지방산과 결합해 있는데, 나머지 하나의 hydroxyl group은 phosphate group과 결합해 있다. 이때 음전하를 띠는 phosphate group의 끝에는 보통 전하를 띠거나 극성을 가진 다른 분자가 결합해 있다. 아래 사진은 choline(콜린)이 결합한 인지질을 보여 준다.
인지질의 한쪽 끝은 인지질로 hydrophobic하고, 한쪽 끝은 phosphate group과 거기 붙어 있는 분자로 인해 hydrophilic하다. 이러한 특성으로 인해 인지질 분자들은 물속에 있을 때 소수성인 부분끼리 모여 phospholipid bilayer(인지질 이중층)을 형성한다.
+) 인지질의 2개의 지방산이 왜 하나는 saturated이고 하나는 unsaturated인지 궁금해서 조사해 봤는데, 불포화 지방산이 있어야 인지질 이중층이 굳어버리지 않고 유동적으로 움직일 수 있다고 한다. 그런데 두 지방산 모두 불포화인 경우는 인지질 이중층이 과도하게 유동적이어서 외부 물질이 너무 쉽게 침투하기 때문에 세포막의 성분으로 부적합하다고 한다. (Reference 2, 3 참조)
Steroids(스테로이드)
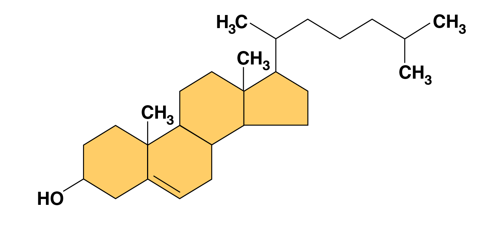
스테로이드는 탄소로 이루어진 4개의 fused ring(축합 고리)가 존재하는 지질의 종류이다. 스테로이드의 종류는 이 fused ring에 달린 chemical groups에 따라 다양하며, 주로 호르몬으로써 생명체 내부에서 신호를 전달하는 역할을 한다. 생명체 내의 대표적 스테로이드인 Cholesterol(콜레스테롤)은 동물 세포막을 구성하는 역할을 하고, 성호르몬의 전구체이다.
Proteins(단백질)
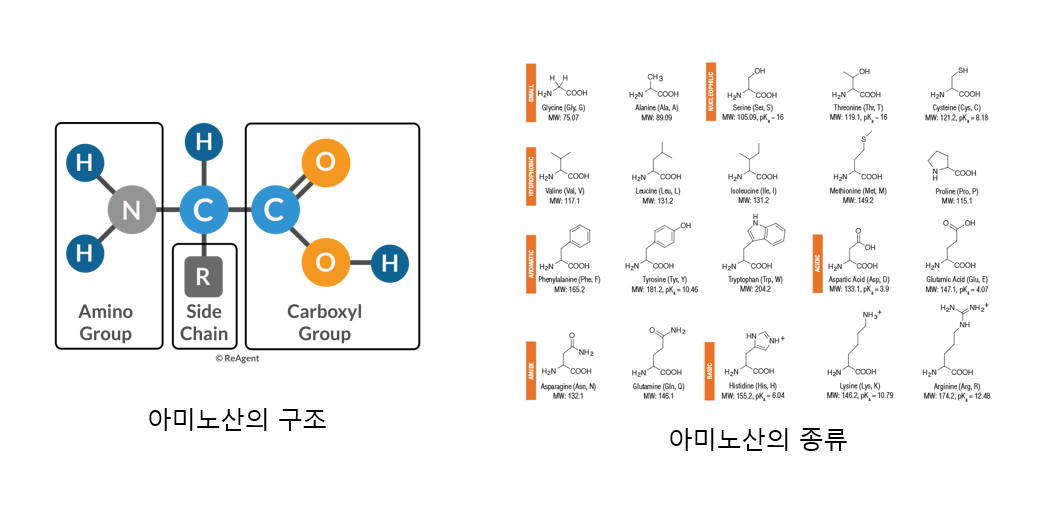
생명체 안에서 가장 중요한 분자 중 하나인 단백질은 20종류의 amino acid(아미노산)으로 구성되는 중합체이다. 아미노산은 중앙에 있는 탄소(α 탄소라고 부름) 하나에 수소, amino group, carboxyl group, 그리고 R group(side chain)이 하나씩 붙은 구조이다. amino group과 carboxyl group은 여러 아미노산이 탈수 반응인 peptide bond를 통해 polypeptide(폴리펩타이드)를 형성하는 데 관여한다. 그리고 R group의 종류에 따라 아미노산의 종류가 결정된다.
+) 아미노산에서 amino group은 양성자를 얻은 형태(-), carboxyl group은 양성자를 잃은 형태(-)의 형태로 존재하기 때문에, 아미노산 분자는 zwitterion(양쪽성 이온)에 해당한다.
Functions of Proteins
단백질의 기능
- Enzymatic proteins: 특정 화학 반응을 촉진 (ex: 소화 효소)
- Defensive proteins: 박테리아, 바이러스 등 외부 병원균 파괴 (ex: 항체)
- Storage proteins: 아미노산 등 물질을 저장 (ex: 계란 흰자에 포함된 오브알부민)
- Transport proteins: 물질을 운반 (ex: 헤모글로빈)
- Hormonal proteins: 생명체의 활동을 조절 (ex: 인슐린)
- Receptor proteins: 화학적 자극에 따른 세포의 반응 조절 (ex: 신경 세포의 수용체)
- Contractile and moter proteins: 움직임 조절 (ex: 섬모, 편모, 액틴, 마이오신)
- Structural proteins: 구조, 형태 지지 (ex: 케라틴, 콜라겐)
Four Levels of Protein Structure
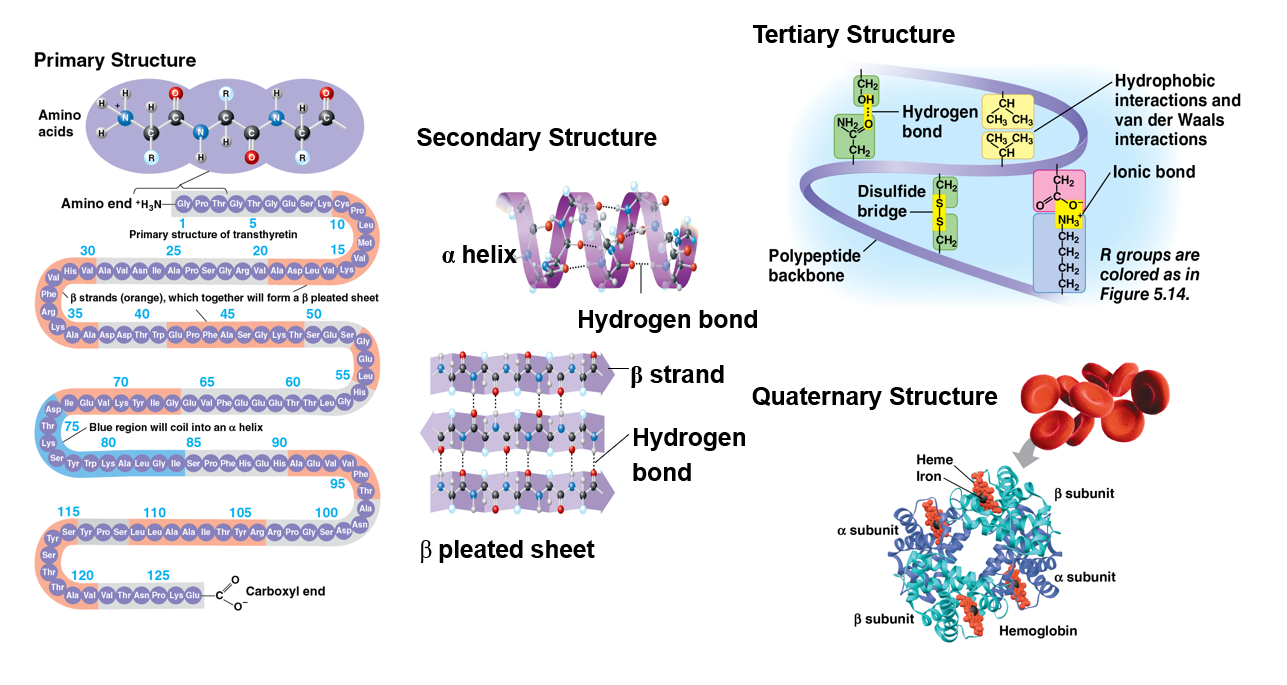
단백질의 구조는 총 4단계로 구분된다.
Primary structure(1차 구조)는 단순히 펩타이드 결합으로 이어진 아미노산들을 직선으로 나열한 것이다.
Secondary structure(2차 구조)는 폴리펩타이드의 backbone(side chain을 제외한 부분)끼리의 수소 결합 패턴으로 인해 자발적으로 만들어지는 모양을 말하는데, 나선형 모양으로 말린 α helix 구조나 병풍 모양으로 이어진 β pleated sheet 구조가 2차 구조에 해당한다.
Tertiary Structure(3차 구조)는 side chain끼리의 상호작용으로 인해 자발적으로 만들어지는 구조를 말한다. 이런 상호작용에는 서로 다른 side chain 사이에서 일어나는 수소 결합, 이온 결합, hydrophobic interaction(무극성인 side chain끼리 뭉치게 되는 현상), 반데르발스 상호작용, Disulfide bridge(황 원자끼리 공유 결합) 등이 있다.
Quaternary Structure(4차 구조)는 다수의 폴리펩타이드 사슬이 합쳐져서 이루는 구조를 말한다. 모든 단백질에 있는 구조는 아니며 콜라겐, 헤모글로빈 등의 단백질이 이 구조를 가지고 있다.
복잡한 단백질의 구조는 Space-filling model, Ribbon model, Wireframe model 등으로 나타낸다.
단백질의 구조는 온도, pH, 용매의 극성 등 환경에 따라 변화할 수 있다. 단백질이 원래의 구조를 잃는 것을 denaturation(변성)이라고 한다. 반대로 원래의 구조로 돌아오는 것을 renaturation(복원)이라고 하는데, 달걀 프라이를 식힌다고 생달걀로 돌아오지 않듯이 모든 단백질이 한번 변성된 후 복원될 수 있는 것은 아니다.
다음 포스팅에서는 핵산에 대해 정리해 보겠다.
References
- Campbell, N. A., Urry, L. A., Cain, M. L. et al. 『Biology: A Global Approach』. 12th ed. Pearson Education Ltd.(2021). p72-83
- Manni, M. M., Tiberti, M. L., Pagnotta, S., Barelli, H., Gautier, R., & Antonny, B. (2018). Acyl chain asymmetry and polyunsaturation of brain phospholipids facilitate membrane vesiculation without leakage. eLife, 7, e34394. https://doi.org/10.7554/eLife.34394
- https://bio.libretexts.org/Bookshelves/Introductory_and_General_Biology/Book%3A_General_Biology_(Boundless)/03%3A_Biological_Macromolecules/3.05%3A_Lipid_Molecules_-_Phospholipids